来源:药智网
大分子、小分子药物扎堆的年代,谁是下一个药企必争之地?或是核素药物。
近日,随着远大医药的全球创新放射性核素偶联药物TLX101中国IND申请获受理,核素药物的热度,再次被点燃。无独有偶,“医药一哥”恒瑞也将注意力转移到核药上:镥[177Lu]氧奥曲肽注射液收到了临床试验批准,将于近期开展临床试验。为什么是核素药物?本文将从核药、放射性医学的发展谈起。1895年11月8日,德国物理学家威廉•康拉德•伦琴(Wilhelm Conrad Roentgen)和以往一样,使用克鲁克斯管做着阴极射线(即电子)方面的研究。当时,管子用黑纸覆盖,房间里很暗,但他注意到房间对面的屏幕在发光,他用手挡住光束时,可以看到他手上的骨头投射在屏幕上。在接下来的几周里,伦琴继续对新射线进行实验。1895年12月28日,他在维尔茨堡的一个物理学会上作了题为《关于新射线的使用》的报告,他将这种新射线命名为X射线,在会上,伦琴展示了那张著名的照片——他妻子手部在X射线曝光30分钟的X射线照片。次年,X射线开始运用于医学领域,形成了放射诊断学的新学科,并奠定了医学影像学基础。1901年,伦琴因X射线方面的工作获得了第一届诺贝尔物理学奖。
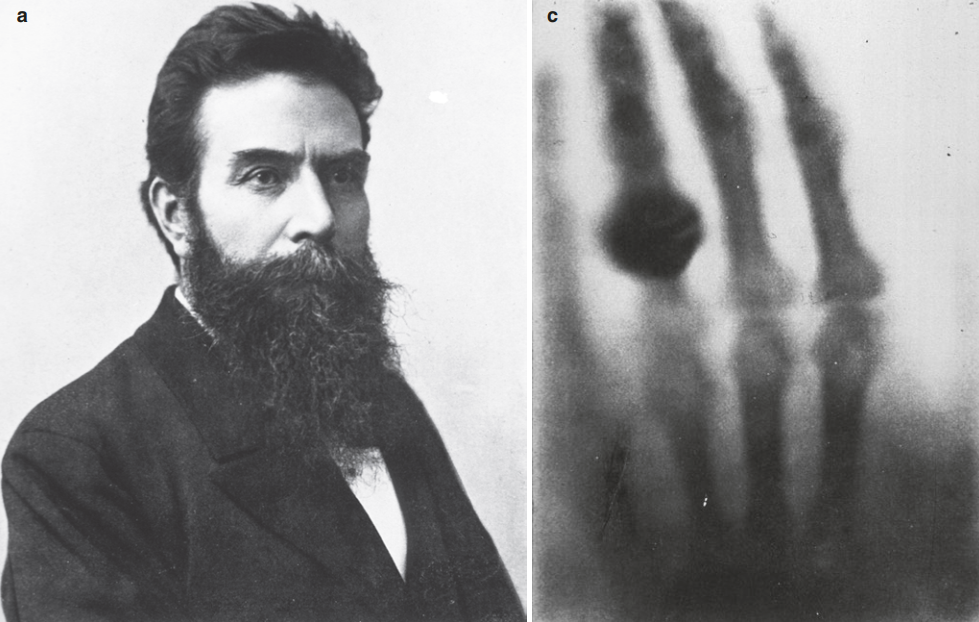
图1 左:伦琴(1845–1923);右:伦琴妻子手部的X光片在得知伦琴发现X射线后,法国物理学家贝克勒尔想起自己之前发现的一种“神秘的射线”。他发现,将含铀元素的K2UO2(SO4)2H2O暴露在阳光下,并将其放在用黑纸包裹的底片上可以使底片曝光。他最初认为太阳的能量被铀吸收,然后发射出X射线。当他将覆盖铀盐的底片被放回了抽屉里,贝克勒尔预计,曝光会非常弱,但是恰恰相反,底片仍然产生很强的曝光。后来,经过多次试验,贝克勒尔确认,这种射线是铀原子的特性,与X射线不同的是,它可以被磁场偏转,因此,它必须由带电粒子组成。贝克勒尔最终证明了天然放射性的存在,并因此被授予1903年诺贝尔物理学奖。
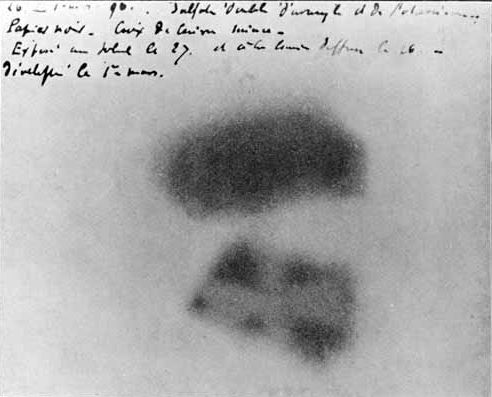
图2 贝克勒尔的底片因暴露在铀盐的辐射中而起雾的图像尽管贝克勒尔因放射性获得诺贝尔奖,但是,“放射性”这一术语本身是由著名的居里夫人(玛丽•斯克洛多夫斯卡•居里)创造的。1897年,玛丽正在为她的博士论文研究寻找一个主题。她被贝克勒尔的工作所吸引,决定利用她丈夫皮埃尔和他的兄弟雅克建造的基于压电效应的电子测量仪,系统地研究铀的“射线”。居里夫人发现,钍发出的射线与铀相同,而且射线的强度不取决于化学成分,只取决于样品中铀或钍的含量。她得出结论,辐射并不取决于分子中原子的排列,而是与原子本身的内部有关。除了铀元素,玛丽和她的丈夫皮埃尔陆续发现了多种放射性元素,包括钍、钋和镭。居里夫妇因其在放射性方面的工作,于1903年获得了诺贝尔物理学奖。

1934年,跟随皮埃尔和玛丽的脚步,他们的女儿伊雷娜和女婿弗雷德里克•约里奥•居里,通过用α粒子照射稳定的核素来创造放射性元素。具体来说,约里奥•居里夫妇用α粒子轰击了一系列元素,包括H、He、Li、B、Be、C、N、O、F、Na、Al、Ca、Mg、Ni和Ag。用钋衰变产生的α粒子轰击铝(Z=13),产生了放射性磷(Z=15)和一个中子。然后他们观察到,这种磷衰变为硅,释放出一个正电子。在与硼进行类似的反应之后,他们能够将正电子发射的放射性核素13N--它发出的辐射的半衰期约为10分钟--凝结在一个单独的容器中,以确认他们实际上已经人为地创造了一种不同的元素。约里奥居里夫妇因人工放射性方面的贡献,获得了1935年的诺贝尔化学奖,这项工作为现代的核医学和放射性药物化学奠定了基础。

大约在同一时间,欧内斯特•劳伦斯在加利福尼亚大学伯克利分校开发了第一个回旋加速器。劳伦斯也在用回旋加速器产生人工放射性,但他没有注意到这些残留的辐射,因为他使用的盖格计数器,同时也在用于其他项目。劳伦斯团队的这项工作,以及1930年代早期约里奥居里的工作促使了1938年在伯克利发现了碘-131(Glenn Seaborg和John Livingood)和锝-99m(Emilio Segre和Glenn Seaborg),并为使用回旋加速器生产正电子发射断层成像(PET)和单光子发射计算机断层成像(SPECT)的放射性核素创造了条件。欧内斯特劳伦斯在1939年获得了诺贝尔物理学奖,以表彰他发明和开发回旋加速器以及用它取得的成果,特别是在人工放射性元素方面的贡献。乔治•德•赫维西(图5)--被称为“核医学之父”,他首先描述了放射性示踪剂原理,该原理是使用放射性核素来研究稳定原子和分子行为的基础。简单地说,示踪剂原理指出,放射性药物可以参与生物过程,但不会改变或扰乱它们。这样,放射性药物有利于对正常和疾病过程进行成像,而不会干扰它们。当然,这一现象的前提是微量的放射性药物可以相对容易地被检测出来。第一个在动物身上进行的放射性示踪剂实验,使用铋-210来跟踪含Bi的抗蚜虫药物在兔子身上的循环。德•赫维西对放射化学的其他开创性贡献,包括他对中子反应的研究。更具体地说,他将镝暴露在中子流中,该元素变得异常活跃,这是中子活化分析的首次展示。基于这些初始实验,他确定了各种辐照位置的相对中子通量,并激活了其他样品,包括铑箔和铕样品。中子活化分析是对固体样品进行元素分析的最强大的无损分析技术。

基于上述获得6项诺奖的早期原子物理研究,放射性核素药物逐渐萌芽。放射性核素药物在医学上的使用,第一个例子为碘元素。碘于1811年在海藻中被发现,1819年首次用于治疗甲状腺肿。1936年,马萨诸塞州综合医院的索尔•赫兹医生设想了放射性碘(RAI)的医疗用途,并问麻省理工学院院长Karl Compton:能否用人工方法使碘具有放射性?这一问题,促成了索尔•赫兹和麻省理工学院物理学家阿瑟•罗伯茨之间的合作。罗伯茨使用中子源生产了I-128(t1/2=25分钟),并研究I-128对兔子甲状腺改变的影响。1936年,使用伯克利回旋加速器,Glenn Seaborg和John Livingood轰击了碲-128,产生了碘-130(t1/2=12小时)和碘-131(t1/2=8天)赫兹和罗伯茨是第一个开发实验数据并将其应用于临床的人。碘-131允许对放射性核素进行长时间的体内追踪。放射性碘的使用,使甲状腺癌从一个几乎肯定的死刑判决,变成了一个总生存率约为85%的疾病。在20世纪30年代末,欧内斯特劳伦斯在伯克利的实验室通过用氘核轰击氧化硼,或多或少地常规生产碳-11(C-11;t1/2=20分钟)。马丁•卡门、萨姆•鲁本和I.L.柴可夫使用碳-11来研究碳水化合物的代谢。但是,碳-11的半衰期为20分钟,这意味着伯克利大学的研究人员在研究方面受到了一定的限制。根据计算,他们知道可以制造碳-14,但他们不知道它的半衰期会是多少,尽管他们预计它的寿命会更长。1940年,卡门和鲁本通过轰击石墨靶获得了碳-14,并计算出碳-14的暂定半衰期为4000年,这个数值与多年后确定的真正半衰期5700年相当接近。由于碳在生命科学中的重要性,碳-14的发现被认为是放射化学的一个开创性时刻。

二战后,原子弹的研制及其在第二次世界大战结束时用于摧毁广岛和长崎,导致1946年成立了原子能委员会(AEC),以促进核化学和放射化学的和平利用。原子能委员会的部分任务,是推动放射性核素在核医学成像和治疗中的应用。1946年,宣布裂变产生的放射性核素,包括碘-131,可以立即从田纳西州橡树岭的曼哈顿项目中获得。来自AEC的资金推动了几个与核医学和分子成像有关的开创性发现,包括开发伽马闪烁术、SPECT相机、PET扫描仪和99Mo/99mTc发生器。除了放射性核素的产生,成像仪器的发展对于核医学的发展也是至关重要的。最初,检测是使用盖革-缪勒计数器进行的,这些计数器在感兴趣的目标上手动移动以测量放射性核素的吸收情况,其评估之一是测量甲状腺的碘吸收率,以诊断结节是良性还是恶性。但是,实际操作起来很困难,因为计数器对碘-131的高伽马辐射不敏感。1960年,本尼迪克特•卡森(Benedict Cassen)开始研究作为闪烁体的金属晶体,通过用钨酸钙调换GM计数器中的探测器来提高灵敏度,以促进碘的增强检测,这一发展导致了闪烁计数器的发展。后来他改用掺铊的碘化钠晶体,增加了光电倍增管(导致灵敏度提高),并使系统自动扫描甲状腺以产生图像。闪烁探测器很快被扩展到其他器官的核图像。下一个进步是直角扫描器的发展,它使扫描器的定位自动化,并成为20世纪50年代至70年代初用于核成像的标准仪器。在这方面,哈尔•安格尔(Hal Anger)发明的伽马相机取得了突破性进展,该相机采用了准直技术,可以一次性观察到整个感兴趣的器官,并增加了光电倍增管阵列以提高检测效率。

1953年,Brownell和Sweet开发了一种用正电子发射的放射性核素,对脑瘤进行定位的多探测器仪器。该设备的工作原理是:将病人相对于探测器移动,每当有重合的事件发生时,就用笔在纸上做一个标记。
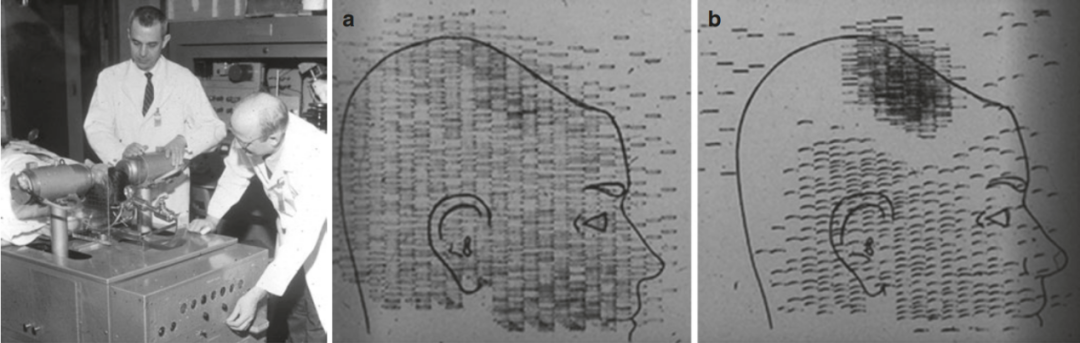
图8 左:由Brownell和Sweet开发的用正电子发射的放射性核素对脑瘤进行定位的多探头仪器。右:该扫描仪的图像显示了脑瘤的存在(图像b)。1966年,在布鲁克海文国家实验室,山本等人开发了第一个用于大脑成像的圆形探测器阵列,由于其形状,被昵称为“缩头乌龟”或“吹风机”。20世纪60年代,David Kuhl和Roy Edwards开发了一台核医学断层成像设备,并提出了纵向和跨轴断层成像的概念。这台机器是现代SPECT系统的前身,证明了断层成像在核医学中的作用。Godfrey Hounsfield接着开发了用于射线摄影的横轴断层摄影,这有助于正电子发射断层摄影(PET)的发展。Ter-Pogossian、Phelps和Hoffman于1975年开发了一台采用滤波背投的PET仪器。

图9 亨利•瓦格纳在华盛顿大学的一台早期PET扫描仪内随着成像设备的发展,放射性标记物的开发也提上日程。2-脱氧-2-[18F]氟-D-葡萄糖—即[18F]FDG或简称FDG,是一种葡萄糖的放射性标记形式,其中一个氟-18原子取代了一个羟基。有了18FDG,就有可能首次将Louis Sokoloff开发的[14C]2-脱氧葡萄糖自显影法应用于临床。虽然[18F]FDG最初是为脑部成像而开发的,但20世纪70年代末和80年代初的其他一些临床前研究表明,这种放射性示踪剂也可用于心肌代谢和肿瘤代谢的成像。1986年,Kurt Hamacher开发了一种使用[18F]氟化物的FDG合成方法,这是一个重要的里程碑。[18F]FDG的突破性发现为探索广泛的疾病和病症打开了大门,包括药物成瘾、饮食失调、注意力缺陷多动障碍(ADHD)、阿尔茨海默病、癫痫和冠状动脉疾病。当然,[18F]FDG PET成像也从根本上重塑了癌症的诊断、分期和治疗监测。由于肿瘤细胞对葡萄糖有很高的需求,[18F]FDG PET扫描可以从周围的健康组织中找出这些“热点”,甚至在检测到解剖学变化之前。
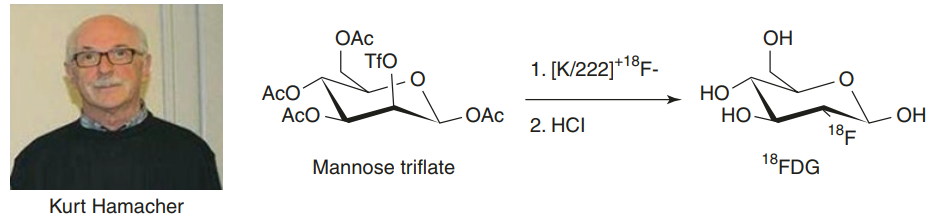
图10 左:库尔特•哈马赫;右:显示[18F]的改进合成方案从核药、放射性医学的发展历程来看,其早期原子物理的基础研究,曾斩获6个诺贝尔奖,而后成功应用在医疗领域,成为科学技术造福人类健康的伟大案例。此外,核成像和靶向放疗在临床上取得的惊人成功,导致了放射性药物化学领域的快速增长。
我们有理由相信,随着科学技术的发展,核素药物、放射性医学将继续大步向前。
声明:本文系转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表我方观点。如涉及作品内容、版权和其它问题,请与我方留言联系,我们将在第一时间删除内容。




















